多学科团队在管理复杂蛋白沉积病例中的角色
蛋白沉积疾病(如系统性淀粉样变性)常涉及多个器官和复杂的分子机制,需要跨专业的协作来实现准确诊断与个体化治疗。本文概述了多学科团队在识别proteinopathy与misfolding现象、利用biomarkers和imaging改进diagnostics与monitoring、并结合cardiology、nephrology与neurology专家的协同管理中的关键角色与实践要点,探讨genomics、proteomics与pharmacology如何为immunotherapy和clinicaltrials提供支持,以提升治疗决策的科学依据。
proteinopathy 与 misfolding 有何机制?
蛋白质错误折叠(misfolding)是多种蛋白沉积疾病的核心病理过程,统称为 proteinopathy。错误折叠的蛋白质聚集形成的纤维可在组织间沉积,导致细胞功能紊乱和器官损伤。理解这些分子过程有助于选择针对性干预,例如抑制聚集、稳定非致病构象或促进清除聚集体的策略。分子层面的研究还推动了诊断工具的发展,使临床团队能更早识别疾病进程。
biomarkers 与 proteomics 在诊断中的作用是什么?
生物标志物(biomarkers)和proteomics技术在早期诊断与风险分层中发挥重要作用。血浆或尿液中的特异性蛋白、轻链或其片段能提示蛋白沉积活动;同时,蛋白组学(proteomics)可揭示新的候选标志物和病理通路。多学科团队应与实验室科学家合作,验证这些标志物在临床情境下的灵敏度与特异度,从而优化诊断流程并支持个体化治疗方案的制定。
imaging、diagnostics 与 monitoring 如何结合?
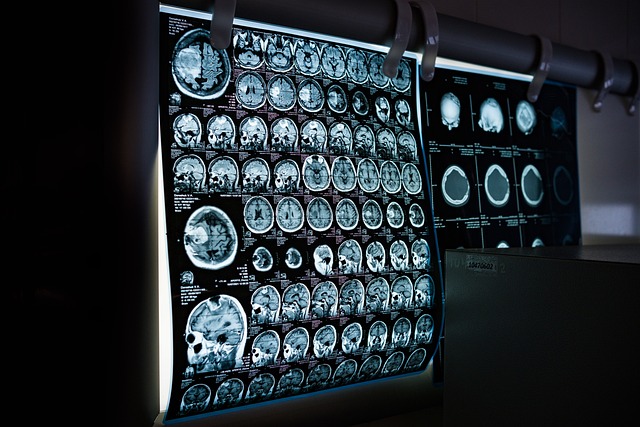
影像学(imaging)与综合诊断(diagnostics)相互补充,用于确定受累器官和评估病情严重程度。心脏磁共振、放射性示踪扫描以及超声在评估器官受累(例如心、肾、神经系统)方面常被采用。持续的监测(monitoring)则依赖于影像随访与生物标志物的动态变化,以评估治疗反应或疾病进展。多学科团队需制定统一的监测指标与时间表,确保影像与实验室数据被及时解读并用于临床决策。
cardiology、nephrology、neurology 团队如何协作?
蛋白沉积经常同时影响多个专科领域,因此cardiology、nephrology与neurology等学科的密切协作十分关键。心脏受累可能导致心力衰竭或传导系统异常,肾脏受累影响液体代谢与药物清除,神经受累则导致感觉或运动功能障碍。通过多学科会诊,团队可以在用药选择、剂量调整、并发症管理和康复计划上达成一致,减少单学科治疗导致的冲突或漏诊。
genomics、immunotherapy、pharmacology 与 clinicaltrials 的角色是怎样的?
基因组学(genomics)能识别遗传易感性或致病突变,从而区分家族性与散发性病例,为靶向治疗提供依据。免疫治疗(immunotherapy)和小分子药物在干预错误折叠或促进沉积体清除方面正在研究与开发中,pharmacology 的药代动力学和药效学研究对剂量优化至关重要。临床试验(clinicaltrials)则为评估新疗法的安全性与有效性提供严格平台,多学科团队应积极参与或利用试验数据将新证据转化为临床实践。
本文仅供信息参考,不应被视为医疗建议。请咨询合格的医疗专业人员以获得个性化建议和治疗。
结论:多学科团队通过整合分子机制研究、先进影像与生物标志物、以及心肾神经科等临床专科的经验,能够在复杂蛋白沉积病例中提供更全面的诊断与管理路径。跨学科的沟通、标准化的监测方案及基于证据的临床试验结果,共同构成了提升疾病管理质量的基石。




